Сколько живут с метастазами в лёгких? Сколько осталось жить? Очаги в легких — что это? Дифференциальная диагностика очаговых изменений в легких при тонкослойной компьютерной томографии
Орган, который чаще всего поражается вторичной онкологией – это легкие . Метастазы в легких занимают второе место среди вторичных онкологических заболеваний после печени. В 35% случаев первичный рак дает метастазы именно в легочные структуры.
Есть два пути распространения метастазов в легкие от первичного очага – гематогенный (через кровь) и лимфогенный (через лимфу). Такое местонахождение метастазов носит опасный для жизни характер, так как выявляются они в большинстве случаев на .
Причины метастазирования легких
Очаги раковой опухоли содержат большое количество аномальных клеток. Соединяясь с кровью и лимфой, раковые клетки распространяются в соседние органы. Там они начинают активно делиться, образуя вторичный очаг онкологического заболевания – метастаз.
Метастазы в легкие могут распространяться практически от любого ракового заболевания.
Наиболее часто встречаются при таких первичных онкозаболеваниях, как:
- Меланома кожи;
- Опухоль молочной железы;
- Рак кишечника;
- Рак желудка;
- Рак печени;
- Рак почки;
- Опухоль мочевого пузыря.
Сокращенное название метастазов – MTC (MTS – от лат. «metastasis»).
Видео — Метастазирование опухолей
Какие могут быть метастазы в легких?
Вторичные очаги могут встречаться как в левом, так и в правом легком. Легочные метастазы подразделяют по признакам на такие группы, как:
- Односторонние и двухсторонние;
- Крупные и мелкие;
- Солитарный (единичный) и множественные;
- Очаговые и инфильтративные;
- Узловые метастазы;
- В виде тканевых тяжей.
При появлении SUSP-подозрения на вторичную онкологию следует пройти обследование.
Симптомы и признаки легочных метастазов
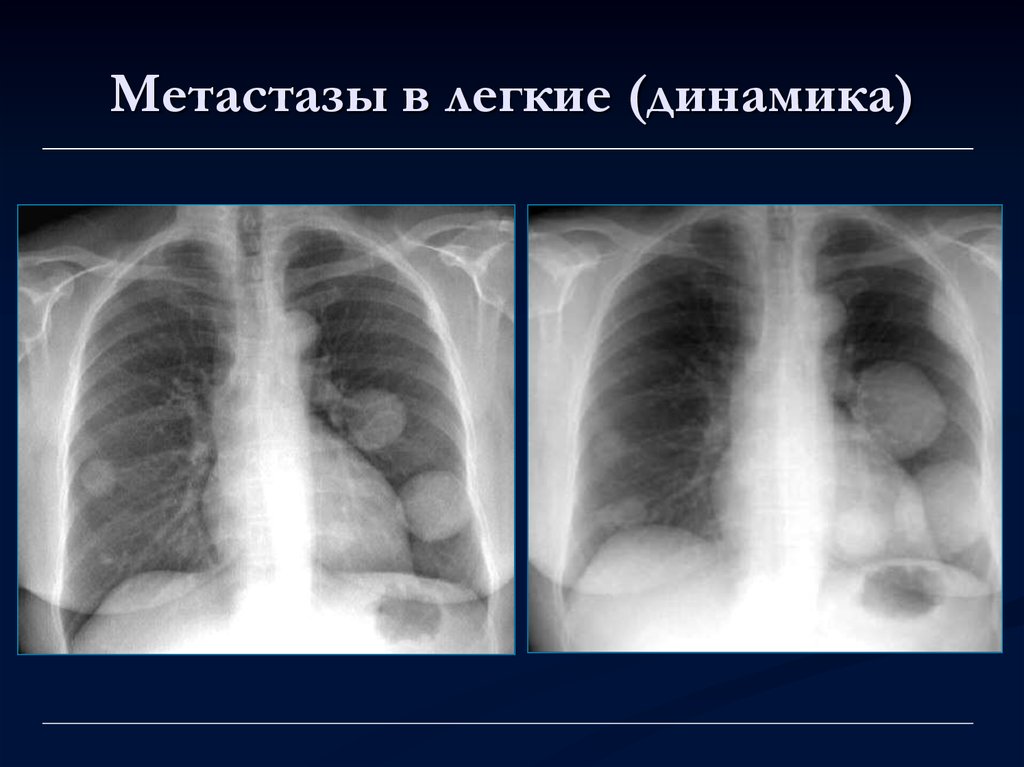 Метастазы в легкие(Динамика) рентген
Метастазы в легкие(Динамика) рентген На ранних стадиях метастазы в легких никак себя не проявляют, болезнь протекает бессимптомно . Распадаясь, клетки раковой опухоли выделяют токсичные вещества, отравляющие организм. Больной обращается за медицинской помощью чаще на последней, .
Наличие вторичных очагов онкологии в легких сопровождается следующими симптомами:
- Частая одышка, появляющаяся не только во время физической нагрузки, но и в состоянии покоя;
- Регулярный сухой кашель, переходящий во влажный, который можно спутать с другим заболеванием;
- Мокрота с примесью крови;
- Боль в грудной клетке, которая не проходит даже с приемом обезболивающих средств. Уменьшить болевой синдром способны лишь наркотические препараты;
- Отек лица и верхних конечностей при локализации вторичного очага в правом легком, головные боли.
Как выглядят метастазы в легких?
 Метастазы в легком можно определить при помощи рентгенографии. Вторичные очаги онкологии на рентгеновских снимках представляются в узловой, смешанной и диффузной форме.
Метастазы в легком можно определить при помощи рентгенографии. Вторичные очаги онкологии на рентгеновских снимках представляются в узловой, смешанной и диффузной форме.
Узловые метастазы проявляются в единичной или множественной форме. Единичные, или солитарные образования, выглядят как округлые узелки, напоминающие первичный очаг онкологии. Чаще всего формируются они в базальной ткани.
Если вторичный генез носит псевдопневманическую форму, то на рентгене он отображается в виде тонких линейных образований.
При метастазировании в плевру на рентгеновских снимках видны крупные бугристые образования, в результате прогрессирования которых ухудшается состояние онкобольного и развивается легочная недостаточность.
Сколько живут с легочными метастазами?
Продолжительность жизни при метастазировании легких зависит от того, как быстро выявлен вторичный рак.
При выявлении у себя хотя бы одного из вышеперечисленных симптомов следует незамедлительно обратиться к врачу и пройти обследование. В медицинской практике бывали случаи обнаружения легочных метастазов задолго до момента выявления первичного очага опухоли.
Прогрессирование вторичной опухоли вызывает организма в целом. Чтобы выявить у себя наличие метастазов, следует знать, как проявляются симптомы заболевания. Первыми признаками прогрессирования вторичного рака в легких являются:
- Снижение аппетита и как следствие массы тела;
- Общее недомогание, быстрая утомляемость и снижение работоспособности;
- Повышение температуры тела, приобретающее хронический характер;
- Сухой кашель при метастазах становится постоянным.
 Вышеперечисленные признаки могут указывать и на первичный . Это довольно опасное заболевание чаще наблюдается у курильщиков. Метастазы при мелкоклеточном раке легкого распространяются стремительно, быстро растут и при несвоевременном их выявлении прогнозы для пациента будут печальными. Первичный рак легкого лечат при помощи химиотерапии. Если провести процедуру своевременно, появляется шанс вылечить онкологию полностью
. Но такая форма заболевания обычно выявляется на последних стадиях, когда вылечить ее уже невозможно. Принимая сильные анальгетики, можно прожить от четырех месяцев до года.
Вышеперечисленные признаки могут указывать и на первичный . Это довольно опасное заболевание чаще наблюдается у курильщиков. Метастазы при мелкоклеточном раке легкого распространяются стремительно, быстро растут и при несвоевременном их выявлении прогнозы для пациента будут печальными. Первичный рак легкого лечат при помощи химиотерапии. Если провести процедуру своевременно, появляется шанс вылечить онкологию полностью
. Но такая форма заболевания обычно выявляется на последних стадиях, когда вылечить ее уже невозможно. Принимая сильные анальгетики, можно прожить от четырех месяцев до года.
Встречаются такие формы первичного рака легкого, которые прогрессируют не так стремительно, как мелкоклеточный рак. Это плоскоклеточный, крупноклеточный рак и аденокарцинома. Эти формы рака лечатся оперативным путем. При своевременном проведении операции, прогноз на выздоровление будет хороший. Если пошли метастазы в другие органы, то пациента ожидает смертельный исход.
Диагностика метастазов в легких
Для выявления наличия вторичного генеза в легком применяются следующие методы диагностирования:
- Рентгенография – исследует структуру тканей легких, выявляет затемнения, месторасположение метастаза и его размеры. Для этого делается два снимка – спереди и сбоку. На снимках множественные метастазы представляются в виде округлых узелков;
- Компьютерная томография – служит дополнением рентгенографии. На КТ видны области, где локализуются метастатические опухоли, каковы их размеры и форма. С помощью КТ выявляют секундарные изменения в легких;
- Магнитно-резонансная томография – назначается людям, ранее подвергавшимся облучению, а также детям. Такое исследование позволяет выявить вторичные новообразования, размеры которых едва достигают 0,3 мм.
Как выглядят метастазы в легких? — Видео
Методы лечения вторичных очагов онкологии в легких
Чем лечить вторичный рак легкого?
В современной медицине для лечения метастазов в легких применяются следующие методы:
- Хирургическое вмешательство – производится удаление пораженного участка. Такой метод лечения эффективен лишь в случае, если имеется одиночное очаговое поражение, поэтому его применяют достаточно редко;
- Химиотерапия – служит дополнением к другим методам лечения. Продолжительность курса химиотерапии зависит от основного метода лечения и самочувствия больного. В медицинской практике химиотерапию применяют совместно с лучевой терапией. Для поднятия уровня лейкоцитов в крови после процедуры назначается дексаметазон;
- Лучевая терапия – позволяет замедлить активный рост раковых клеток и уменьшает боли. Облучение производится в стационарных условиях дистанционным способом;
- Гормональная терапия – применяется при наличии гормоночувствительного первичного очага в предстательной или молочной железах. Служит дополнением к основной терапии;
- Радиохирургия – (пучка лучей) удалять труднодоступные опухоли.
Инвалидность при раке легкого оформляется в случае удаления одной доли.
Лечатся ли метастазы народными средствами?
 Лечение вторичной онкологии в легком можно производить и народными методами. Самым распространенным народным средством является чистотел. Необходимо столовую ложку высушенной травы залить кипятком и настаивать в термосе около полутора часа. Затем настой процедить и принимать его дважды в день по две столовые ложки до еды.
Лечение вторичной онкологии в легком можно производить и народными методами. Самым распространенным народным средством является чистотел. Необходимо столовую ложку высушенной травы залить кипятком и настаивать в термосе около полутора часа. Затем настой процедить и принимать его дважды в день по две столовые ложки до еды.
В заключение можно сказать, что встречаются различные формы поражения легких онкологией. Это и первичный рак, и метастазы, перешедшие из других очагов. Болезнь может протекать бессимптомно, а это означает, что больной может обратиться за помощью тогда, когда лечение уже не даст нужного результата.
Прогноз на выживаемость зависит от стадии заболевания, вида, формы и местоположения опухолей .
И.Е. Тюрин
Очаговые образования в легких представляют собой самостоятельный рентгенологический и клинический синдром; в большинстве случаев они протекают бессимптомно и выявляются при профилактических рентгенологических исследованиях.
Одиночный очаг в легких (ООЛ) определяют как локальный участок уплотнения легочной ткани округлой или близкой к ней формы диаметром до 3 см. Это международное определение отличается от традиционного отечественного представления о легочных очагах, источником которого является фтизиатрическая практика (в классификации туберкулеза легких размеры очагов не превышают 1 см, а уплотнения большего размера определяются как инфильтраты, туберкуломы и другие виды изменений).
Максимальный размер одиночного очага, равный 3 см, соответствует принятой в настоящее время схеме стадирования немелкоклеточного рака легкого, в которой очаги такой величины относят к стадии Т1 опухолевого роста. Очаги в легочной ткани могут быть единичными (в количестве от 2 до 6 включительно) или множественными. Последние относятся к рентгенологическому синдрому диссеминации и обычно рассматриваются в контексте дифференциальной диагностики интерстициальных (диффузных паренхиматозных) заболеваний легких.
Единичные очаги занимают промежуточное положение, а их оценка в значительной степени определяется конкретной клинической ситуацией (например, скрининг рака легкого, злокачественная опухоль внегрудной локализации в анамнезе и т.д.). Наличие именно одиночного очага является одним из основных критериев синдрома ООЛ.
Правильная характеристика ООЛ остается важной клинической проблемой в торакальной радиологии и в респираторной медицине в целом. Известно, что 60-80% резецированных ООЛ представляют собой злокачественную опухоль. Среди всех ООЛ, выявляемых при рентгенологическом исследовании, частота опухолей значительно меньше (обычно она не превышает 50%), однако и в этом случае правильная оценка изменений в легких имеет большое значение для пациента.
Основной задачей лучевого исследования при ООЛ является неинвазивная дифференциальная диагностика злокачественного и доброкачественного процесса, а также выявление среди них форм туберкулеза легких. В ряде случаев это возможно на основании характерных признаков, обнаруживаемых при рентгенографии или рутинной компьютерной томографии (КТ).
Тем не менее специфичность большинства из этих симптомов низка, поэтому для правильной оценки ООЛ необходимо привлечение дополнительных методик и альтернативных технологий. К ним можно отнести оценку скорости роста очага в легком, анализ вероятностных факторов злокачественности, динамику накопления контрастного вещества при КТ и 18-фтордезоксиглюкозы (18-ФДГ) при позитронно-эмиссионной томографии (ПЭТ), а также морфологическое исследование материала, полученного при трансторакальной игловой аспирационной биопсии или видеоторакоскопии.
Очевидно, что в повседневной клинической практике вряд ли может существовать единый алгоритм дифференциальной диагностики ООЛ для всех пациентов и для всех клинических ситуаций, а задачей любых клинических рекомендаций является точная оценка возможностей, предоставляемых отдельными диагностическими методами и их сочетаниями.
Выявление одиночных очагов в легких . До настоящего времени методом первичного выявления очагов в легочной ткани остается обычное рентгенологическое исследование – рентгенография или флюорография. Одиночные очаги обнаруживаются в 0,2-1,0% всех рентгенологических исследований грудной клетки. На обзорных рентгенограммах или флюорограммах редко можно выявить одиночный очаг размером <1 см.
Даже более крупные очаги могут быть пропущены из-за интерпозиции анатомических структур (сердечная тень, корни легких, ребра и др.) или наличия так называемых отвлекающих факторов, например аномалии развития или патологии сердца. Более 90% всех ООЛ, видимых на рентгенограммах, могут быть обнаружены ретроспективно на предшествующих снимках давностью 1 или даже 2 года.
Всё большее значение в диагностике легочных очагов приобретает КТ, которая может проводиться как при подозрении на наличие ООЛ по данным рентгенографии, так и по другим показаниям (для исключения пневмонии, при обследовании больных хронической обструктивной болезнью легких и эмфиземой и т.д.). В целом КТ позволяет выявить в 2-4 раза больше очагов в легочной ткани, чем рентгенография, при этом средний размер выявляемых очагов в 2 раза меньше.
Однако КТ также не является абсолютным методом диагностики. Результаты скрининга рака легкого с помощью низкодозной КТ показывают, что основными причинами пропуска патологии являются небольшие размеры очагов (чувствительность КТ в выявлении очагов размером <5 мм равна 72%), низкая плотность очагов по типу “матового стекла” (чувствительность 65%) и их локализация в центральных зонах легкого (чувствительность 61%). В среднем частота пропусков патологии при первичном КТ-скрининге может достигать 50%. В выявлении ООЛ размером >1 см чувствительность КТ обычно выше 95%.
Повышению точности КТ в выявлении мелких очагов в легочной ткани способствует ряд специальных методик – программ для компьютерной диагностики очагов (computer-aided diagnosis, CAD) и программ трехмерных реформаций, таких как проекции максимальных интенсивностей (maximum intensity projections, MIP) и объемный рендеринг (volume rendering technique, VRT).
Анатомическая оценка одиночных очагов в легки х. Оценка скиалогических особенностей ООЛ по данным рентгенографии или КТ имеет большое значение для дифференциальной диагностики. Очаги можно разделить по размерам, характеру контуров, структуре, плотности, состоянию окружающей легочной ткани. Практически все признаки имеют вероятностное значение, будучи более или менее характерными для доброкачественного или злокачественного процесса.
Лишь в исключительных случаях на основании данных лучевого исследования можно предположить нозологический диагноз. Так, наличие жировых включений типично для гамартомы, кольцевидное или тотальное обызвествление очага обычно наблюдается при туберкуломах, наличие приводящего и отводящего сосуда наряду с типичным усилением при контрастировании отличает артерио-венозные мальформации.
Локализация очага в легочной ткани не имеет принципиального значения, так как исключения и совпадения наблюдаются здесь слишком часто. Более 70% очагов рака легкого расположено в верхних долях легких, причем чаще в правом легком, чем в левом. Эта локализация типична и для большинства туберкулезных инфильтратов. Нижнедолевая локализация характерна для рака легкого, возникающего на фоне идиопатического легочного фиброза. Туберкулезные инфильтраты, расположенные в нижних долях, чаще локализуются в их верхушечных сегментах.
Очаги в легочной ткани могут иметь различные контуры: ровные или неровные (волнистые, бугристые), четкие или нечеткие (лучистые или размытые за счет зоны “матового стекла” по периферии). В целом нечеткие и неровные контуры более характерны для злокачественных новообразований, хотя могут наблюдаться и при воспалительных инфильтратах. В одном из исследований, основанном на данных высокоразрешающей КТ (ВРКТ), злокачественными были все очаги, имевшие ободок низкой плотности, 97% очагов с выраженной лучистостью контуров, 93% очагов с неровными и 82% – с волнистыми контурами.
При размерах очага >1 см такие контуры служат веским аргументом в пользу злокачественного процесса и, следовательно, показанием для морфологической верификации. Четкие ровные контуры могут наблюдаться при доброкачественных заболеваниях, но постоянно наблюдаются также при одиночных метастазах, отдельных гистологических формах рака легкого (плоскоклеточный, мелкоклеточный) и легочных карциноидах.
В одном из исследований среди очагов, имевших четкие волнистые контуры, частота злокачественных опухолей достигала 40%. Поэтому округлая форма и четкие контуры очага сами по себе не являются признаками доброкачественности процесса и не могут служить причиной для завершения диагностического процесса.
Плотность одиночных очагов в легких, определяемая при КТ, позволяет разделить все очаги на три группы :
- очаги по типу “матового стекла”;
- смешанные или частично солидные очаги;
- очаги солидного типа.
Очаги по типу “матового стекла” отличаются низкой плотностью, на их фоне видны стенки бронхов, контуры сосудов и элементы измененного легочного интерстиция. Они наблюдаются при недеструктивных воспалительных процессах, атипичной аденоматозной гиперплазии и высокодифференцированных аденокарциномах.
Морфологическая основа данного феномена заключается в утолщении межальвеолярных перегородок на ограниченном участке при сохранении воздушности альвеол, что может возникать за счет воспалительной инфильтрации, фиброзных изменений или частичного заполнения альвеол экссудатом. При развитии аденокарциномы (в том числе и бронхиолоальвеолярной) опухолевые клетки располагаются вдоль стенок альвеол, длительное время не заполняя их просвет. В результате возникает опухолевый очаг по типу “матового стекла”, который в большинстве случаев не виден на рентгенограммах и линейных томограммах.
Очаги смешанного или частично солидного типа характеризуются наличием более плотного участка в центре и зоны низкой плотности по типу “матового стекла” по периферии. Такие очаги обычно возникают вокруг старых рубцов в легочной ткани, в том числе и посттуберкулезных. В большинстве случаев они представляют собой разрастание железистой опухоли. До 34% несолидных очагов представляют собой злокачественную опухоль, а среди очагов частично солидного типа размером <1,5 см этот показатель достигает 50%.
Солидные очаги имеют типичную структуру локального уплотнения округлой формы, мягкотканной плотности, с различными контурами. Они могут наблюдаться практически при любом патологическом процессе в легочной ткани.
Структура ООЛ, выявляемая при КТ, может быть различной: однородной, с участками низкой плотности, обусловленными некрозом, с воздушными, жировыми, жидкостными и высокоплотными включениями, с видимыми просветами бронхов. Ни один из этих симптомов не является специфичным для какого-либо конкретного патологического процесса, за исключением уже упоминавшихся жировых включений при гамартомах.
При обычной рентгенографии удается выявить лишь часть обызвествлений и включений воздуха в виде полостей, воздушных ячеек (сот, пор) или просветов бронхов. При КТ обызвествления в ООЛ выявляют в 2 раза чаще, чем при обычном рентгенологическом исследовании. Обызвествления могут быть очаговыми (по типу “воздушной кукурузы”), слоистыми (в том числе в виде обызвествления капсулы очага) и диффузными, занимающими весь объем очага.
Такие обызвествления типичны для доброкачественных процессов. Исключение составляют лишь метастазы костных сарком, железистого рака толстой кишки и яичников после химиотерапии и легочные карциноиды. Во всех остальных случаях вероятность неопухолевого процесса исключительно велика. В злокачественных очагах, в том числе в аденокарциномах, нередко выявляют точечные или аморфные, без четких контуров, включения кальция.
В целом частота обызвествлений в периферических раковых опухолях по данным КТ достигает 13%. Исключением из этого правила являются очаги по типу “матового стекла”, выявляемые при КТ, и очаги любой структуры на рентгеновских снимках, представляющие собой бронхиолоальвеолярный рак. Пациенты с такого рода очагами требуют более длительного наблюдения.
Другим фактором, ограничивающим возможности динамического или ретроспективного наблюдения, являются размеры ООЛ <1 см. Удвоение объема опухолевого очага диаметром 5 мм приводит к увеличению его диаметра всего на 1,5 мм (до 6,5 мм). Оценка подобной динамики находится за пределами возможностей не только традиционной рентгенографии, но и в большинстве случаев КТ.
В связи c этим большое значение сегодня придается компьютерной оценке объема очагов по данным спиральной КТ, когда компьютер строит трехмерные модели выявленных очагов и сравнивает их объемы. Эта методика, являющаяся составной частью CAD-систем, рассчитана на солидные очаги и не может с уверенностью использоваться для очагов по типу “матового стекла” и очагов частично солидного типа.
Вероятностный анализ . Клиническая оценка пациентов с выявленным ООЛ имеет большое значение в дифференциальной диагностике, хотя нередко недооценивается лечащими врачами и рентгенологами. Вероятностный анализ учитывает количественное значение факторов риска или их отсутствия для предположения о характере ООЛ. Используя подобные расчеты, можно определить индивидуальный риск злокачественной опухоли в конкретной клинической ситуации. При этом учитываются как клинические факторы, так и рентгенологические симптомы.
Наиболее важными факторами, свидетельствующими в пользу злокачественного процесса, являются :
- толщина стенки полости в очаге >16 мм;
- неровные и нечеткие контуры очага при КТ;
- кровохарканье;
- злокачественные опухоли в анамнезе;
- возраст >70 лет;
- размеры очага 21-30 мм;
- время удвоения объема очага <465 дней;
- тень малой интенсивности при рентгенографии.
Большое значение имеют также фактор длительного курения и аморфные обызвествления в очаге, выявляемые при КТ. К сожалению, существующие модели вероятностного анализа не включают данные современных технологий, таких как динамическая КТ и ПЭТ.
Характеристика одиночных очагов в легких при динамической КТ . Оценка кровоснабжения ООЛ при динамической спиральной КТ показала свою эффективность в многочисленных исследованиях. Известно, что плотность ООЛ при нативном исследовании колеблется в широких пределах и не имеет какого-либо диагностического значения (кроме включений жира и кальция).
При динамической КТ патологические образования, имеющие собственную сосудистую сеть, активно накапливают внутривенно введенное контрастное вещество, при этом плотность их повышается. Типичным примером таких очагов являются злокачественные опухоли. Наоборот, образования, лишенные собственных сосудов или заполненные бессосудистым содержимым (гной, казеоз, экссудат и т.п.), не изменяют свою плотность. Такие очаги могут быть представлены туберкуломами, кистами, абсцессами и другими патологическими процессами.
Наибольшее значение методика динамической КТ при ООЛ имеет в регионах с высокой заболеваемостью туберкулезом, поскольку позволяет точно разграничить злокачественные опухоли и туберкуломы. Динамическая КТ выполняется в виде серии томографических срезов через патологическое образование, которые выполняются исходно, во время введения контрастного вещества и через 1, 2, 3 и 4 мин после него. Измерение плотности очага проводится в зоне интереса (ROI), которая занимает не менее 3/4 площади среза очага.
Для разграничения доброкачественных и злокачественных процессов необходимо выбрать так называемый порог усиления – числовое значение коэффициента ослабления, превышение которого позволяет предположить наличие злокачественной опухоли. Таким порогом, определенным эмпирически в крупном многоцентровом исследовании, является 15 HU. При таком пороге усиления чувствительность динамической КТ в выявлении злокачественных опухолей достигает 98%, специфичность – 58%, а общая точность – 77%.
Несмотря на высокую чувствительность в отношении злокачественных опухолей, методика имеет ряд недостатков. К ним относят трудности оценки небольших (<1 см) очагов, низкую специфичность, технические ошибки, связанные с дыханием пациента и артефактами от костных структур и контрастного вещества. Эти недостатки частично компенсированы внедрением в клиническую практику многослойной КТ (МСКТ).
В большинстве исследований проводится оценка накопления, но не выведения контраста из очагов. Между тем показано, что повышение плотности более чем на 25 HU и быстрое уменьшение ее на 5-30 HU при использовании МСКТ типично для злокачественных новообразований. Доброкачественные очаги отличаются повышением плотности менее чем на 25 HU (в ряде случаев плотность повышается более чем на 25 HU, однако затем наблюдается ее быстрое снижение более чем на 30 HU или отсутствие снижения плотности вообще). Если выбрать порог усиления в 25 HU и диапазон снижения плотности 5-30 HU, то чувствительность, специфичность и общая точность методики в отношении злокачественных опухолей составят 81-94, 90-93 и 85-92% соответственно.
Метаболическая характеристика одиночных очагов в легких при ПЭТ . Все методы анатомической визуализации, включая рентгенологический, ультразвуковой, КТ и магнитно-резонансную томографию, ориентированы на макроскопические признаки легочных очагов, большинство из которых недостаточно специфичны. В последние годы всё большее распространение получают исследования метаболических характеристик очага с помощью ПЭТ с 18-ФДГ. Злокачественные опухоли отличаются более высокой метаболической активностью, что характеризуется быстрым и значительным накоплением 18-ФДГ в очаге и длительным ее сохранением.
Многочисленные исследования показали, что ПЭТ отличают высокая чувствительность (88-96%) и специфичность (70-90%) в отношении злокачественных очагов в легких. Еще более высокие результаты получают при сочетанном использовании ПЭТ и КТ-сканеров – ПЭТ/КТ-исследовании с последующим совмещением метаболической и анатомической картины. Ложноположительные результаты ПЭТ наблюдаются при активных воспалительных процессах, в том числе при активном туберкулезе легких.
Отрицательный результат ПЭТ считается исключительно важным для исключения злокачественной природы ООЛ, однако ложноотрицательные заключения могут наблюдаться при первичных опухолях легких по типу “матового стекла” и очагах размером <7 мм. Поэтому данные ПЭТ должны обязательно сопоставляться с результатами КТ для более точного понимания их клинического значения. В целом в настоящее время ПЭТ является наиболее точным методом для разграничения доброкачественных и злокачественных очагов в легочной ткани размером >1 см.
Биопсия . Для очагов, имеющих анатомические или метаболические признаки злокачественности, необходима морфологическая верификация до начала какого-либо лечения. Это правило обязательно, поскольку тактика обследования и лечения при первичной немелкоклеточной, мелкоклеточной и метастатической опухоли в легком может быть совершенно разной.
Существует несколько методов забора материала из легочного очага, в том числе трансторакальная игловая аспирация и биопсия, трансбронхиальная биопсия, видеоторакоскопическая резекция очага с последующей биопсией, открытая биопсия при миниторакотомии. Трансторакальная биопсия проводится под контролем рентгеноскопии, КТ, а в последние годы – всё чаще при КТ-флюороскопии. Трансбронхиальная биопсия обычно выполняется под контролем рентгеноскопии. Пункция очагов, прилежащих к грудной стенке, может быть выполнена с помощью ультразвукового наведения.
Трансторакальная тонкоигольная аспирационная биопсия легочных очагов, проводимая с помощью КТ и КТ-флюороскопического наведения, в отношении злокачественных новообразований имеет чувствительность 86% и специфичность 98%, однако ее чувствительность в отношении очагов <7 мм в диаметре составляет лишь 50%. Все пункционные методы биопсии отличаются низкой чувствительностью при лимфомах с поражением легочной ткани (12%) и доброкачественных образованиях (до 40%).
В этих случаях предпочтение следует отдать толстоигольной биопсии, чувствительность которой в этих категориях достигает 62 и 69% соответственно. Осложнения при трансторакальной биопсии (преимущественно пневмоторакс и внутриплевральное кровотечение) возникают примерно у 25% пациентов. После биопсии нуждаются в установке дренажа не более 7% пациентов, поэтому такая процедура может выполняться в амбулаторных условиях. Противопоказаниями к проведению биопсии служат тяжелая дыхательная и сердечная недостаточность, выраженная эмфизема легких, расположение очага в непосредственной близости от диафрагмы или перикарда.
Трансбронхиальная биопсия может выполняться при локализации очага в прикорневых отделах, особенно в случаях так называемой “централизации” злокачественной опухоли. При этом эндобронхиальный компонент может быть выявлен при бронхологическом исследовании. Другим вариантом верификации является браш-биопсия, при которой материал забирается с внутренней поверхности бронха, расположенного рядом с очагом или внутри него. Для проведения такой процедуры обязательной является предварительная оценка очага и прилежащих к нему бронхов при ВРКТ.
Алгоритмы диагностики при одиночных очагах в легких . В настоящее время не существует единого подхода к определению характера ООЛ. Очевидно, что у пациентов с высоким риском злокачественной опухоли оптимальным подходом является возможно более ранняя морфологическая верификация диагноза при трансторакальной биопсии. У пациентов с низким риском злокачественного процесса более рационально проводить динамическое наблюдение.
В любом случае современный подход требует выполнения ВРКТ при обнаружении ООЛ при рентгенографии, флюорографии или обычной КТ. Другим обязательным шагом становится поиск и изучение любых предшествующих снимков легких.
Результатом этих действий может быть выделение группы пациентов с очевидно доброкачественным процессом, о чем свидетельствуют: отсутствие динамики очага на протяжении >2 лет, наличие “доброкачественных” обызвествлений, включений жира (гамартома) или жидкости (киста) в очаге по данным КТ Для этих пациентов необходимо только наблюдение. Сюда же относятся случаи артерио-венозных мальформаций и других сосудистых изменений, а также воспалительные процессы в легких (округлый туберкулезный инфильтрат, туберкулома, мицетома и др.), требующие специфического лечения.
Второй возможный результат – обнаружение признаков злокачественного процесса (очаг >1 см с лучистыми неровными контурами, очаги по типу “матового стекла” и смешанного солидного типа, которые должны расцениваться как потенциально злокачественные), при которых необходима морфологическая верификация в условиях специализированного лечебного учреждения.
Все остальные случаи расцениваются как промежуточные или неопределенные. Наиболее многочисленную группу среди них составляют пациенты с впервые выявленными ООЛ (в отсутствие рентгенологического архива) размером >10 мм, мягкотканной плотности, с относительно четкими ровными или волнистыми контурами, без каких-либо включений по данным КТ. Уточнение природы ООЛ у таких пациентов может осуществляться с помощью биопсии, динамической КТ, ПЭТ и ПЭТ/КТ Выжидательная тактика и динамическое наблюдение допустимы здесь лишь в исключительных случаях, обоснованных клинической целесообразностью.
Отдельную группу составляют пациенты с выявленными при КТ некальцинированными очагами размером <10 мм. Обычно их обнаруживают при КТ, проведенной для исключения пневмонии или уточнения характера эмфиземы, при трудностях интерпретации рентгеновских снимков и т.д. Такие очаги обычно не видны при обычном рентгенологическом исследовании, их верификация с помощью трансторакальной биопсии малоэффективна, а использование ПЭТ сопряжено с большим количеством ложноотрицательных результатов.
Помимо этого вероятность злокачественного процесса при очагах диаметром <5 мм не превышает 2%. В связи с этим принята следующая тактика. Очаги размером <5 мм не требуют никакого динамического наблюдения, таким пациентам может быть рекомендовано обычное профилактическое обследование (флюорография или КТ) через 1 год. Очаги размером 5-10 мм требуют проведения контрольной КТ через 3, 6, 12 и 24 мес. При отсутствии динамики наблюдение прекращается, а любые изменения формы, размеров или количества очагов служат показанием для биопсии.
Таким образом, дифференциальная диагностика при выявлении одиночного очага в легких является сложной клинической задачей, которая в современных условиях решается с помощью различных методов лучевой и инструментальной диагностики.
Плотность легочной ткани в базальных сегментах может понижаться до –900…--950 HU, что свидетельствует о развитии эмфиземы. Эмфизематозные буллы могут образовываться и в верхних долях вдоль поверхности костальной, медиастинальной и междолевой плевры. Они приводят к оттеснению очагов и инфильтратов в центр легочной ткани, к корню легкого. В заключительной стадии эти изменения можно определить как «сотовое легкое» (рис. 8).
Рис. 8. Высокоразрешающая КТ. Исход хронического гематогенно-диссеминированного туберкулеза в «сотовое легкое» с фиброзом и большим количеством полиморфных очагов с обеих сторон.
Лимфогенные туберкулезные диссеминации отличаются особенностями, на основании которых можно предполагать их патогенетический механизм развития. К ним относятся преобладание очаговых высыпаний (чаще милиарных) в средних отделах, на уровне корней, и меньшая их выраженность в верхушечных и базальных сегментах легких. Найбольшие изменения локализуются в передних и задних сегментах верхних долей, в верхушечных сегментах нижних долей, а также в язычковых сегментах и средней доле. Другим отличительным признаком лимфогенной природы диссеминации является неравномерность поражения легких с чередованием измененных и нормальных участков. При этом расположение очагов и преобладание интерстициальных изменений соответствует границам определенного лимфатического коллектора глубокого или поверхностного. В большинстве случаев в патологический процесс вовлекается глубокая лимфатическая сеть легкого, в результате чего изменения локализуются в глубине легочной ткани, вдоль сосудов и бронхов (рис. 9).


Рис. 9. Высокоразрешающая КТ. Лимфогенный диссеминированный туберкулез. С обеих сторон множественные мелкие очаги на фоне интерстициальных изменений. Распределение очагов в легочной ткани неравномерное, с вовлечением в патологический процесс преимущественно глубокой лимфатической сети (стрелки).
В каждой доле можно выявить один или несколько изолированных участков очагового уплотнения легочной ткани неправильной формы, широким основанием обращенных к плевре, а вершиной к корню легкого. Нечеткие очертания сосудов, линии Керли в сочетании с увели-
ченными лимфатическими узлами корней легких и средостения, также признаки лимфогенной диссеминации. В тех случаях, когда патологические изменения располагаются преимущественно в кортикальных отделах легких, на границе поверхностной и глубокой лимфатической сети, очаги располагаются в виде широкой полосы вдоль грудной стенки и средостения. При этом глубокие и прикорневые отделы легких остаются малоизмененными.
ОЧАГОВЫЙ ТУБЕРКУЛЕЗ
Очаговый туберкулез легких характеризуется наличием немногочисленных очагов, преимущественно продуктивных, на ограниченном участке и занимающих 1-2 сегмента одного или обоих легких. К нему относятся как недавно возникшие, свежие процессы с размером очагов менее 10 мм, так и более давние (фиброзно-очаговые) образования, но с явно выраженными признаками активности процесса. Применение КТ необходимо в тех случаях, когда при обычном рентгенотомографическом исследовании наличие очагов сомнительно или не удается детально оценить их характер. Очаги располагаются в респираторном отделе и в глубине легочной ткани перибронхиально. Типичная их локализация – верхушечный и задний сегменты верхней доли, реже в верхушечном сегменте нижней доли. Чаще очаги имеют полиморфный характер, типично сочетание одного или двух крупных очагов с большим количеством мелких и средних (рис.10).


Рис.10. Высокоразрешающая КТ. В верхней доле левого легкого полиморфные очаги с нечеткими контурами, часть их сливается друг с другом (стрелка).
Очаги обычно имеют однородную структуру, в центре некоторых крупных могут быть видны поперечные просветы бронхов, которые от полостей деструкции отличаются соответствием размеров просветления калибру бронхов такого же порядка на аксиальных снимках и изменением формы при реконструкциях. Истинные полости в очагах имеют более крупные размеры, эксцентричное расположение, выявляются только при высокоразрешающей КТ. При активизации туберкулезного процесса контуры крупных очагов становятся неровными и нечеткими, мелкие очаги диаметром 1-3 мм располагаются вокруг. Они локализуются преимущественно в стенках вторичных легочных долек и внутридольковых перегородок (межацинозных). Развитие лимфостаза приводит к утолщению и уплотнению этих интерстициальных структур, повышению плотности легочной ткани при денситометрии.

Рис. 11. Высокоразрешающая КТ. Прицельная реконструкция правого легкого. В S 1-2 полиморфные очаги с тенденцией к слиянию и нечеткими контурами, в некоторых с субплевральным расположением мелкие полости распада (стрелка).
Длительное течение очагового туберкулеза, особенно на фоне антибактериальной терапии, приводит к существенному изменению компьютерно-томографической картины. Наряду с очаговыми изменениями в легочной ткани появляются участки панлобулярной и парасептальной эмфиземы, мелкие эмфизематозные буллы, а также фиброзные линейные тяжи, направленные из зоны патологических изменений к плевре.

Рис. 12. Высокоразрешающая КТ. Прицельная реконструкция левого легкого. Очаговый туберкулез, хроническое течение. Крупные очаги с четкими контурами на фоне участков вздутия легочной ткани (стрелки).
Объем пораженных сегментов постепенно уменьшается за счет развития локального пневмосклероза. В решении вопроса о длительности существования туберкулезного процесса высокоразрешающая КТ имеет значительные преимущества перед обычным рентгенологическим исследованием. Объективное измерение курсором уменьшения размеров крупных очагов, исчезновение или уменьшение количества мелких очагов при динамическом наблюдении, свидетельствуют о положительной динамике патологического процесса. Исходом очагового туберкулеза у большинства больных является образование мелких линейных рубцов, включения извести в очаги, полости буллезной эмфиземы и локальное утолщение костальной плевры. В отличие от начальных изменений, мелкие очаги в интерстиции стенок долек отсутствуют, что имеет значение для определения активности туберкулезного процесса.
Компьютерная томография (кт) - это один из методов исследования человеческого тела на предмет выявления различных образований, и изменений во внутренних органах и тканях организма, с целью постановки, в дальнейшем, максимально точного диагноза.
Данный метод диагностики является наиболее современным и одним из самых точных. Его суть заключается в воздействии на тело человека рентгеновских лучей, и последующем, после их прохождения сквозь тело пациента, компьютерном анализе.
Именно таким способом удаётся:
- За минимальные сроки и с максимальной точностью понять какое заболевание поразило лёгкие больного;
- Определить на какой стадии находится заболевание;
- Дать адекватную оценку общего состояния лёгких (определение их плотности, диагностика состояния альвеол, измерение дыхательного объёма);
- Проанализировать состояние всех, даже самых мелких лёгочных сосудов, сердца, аорты, лёгочной артерии, верхней полой вены, трахеи, бронхов, а так же лимфатических узлов расположенных в грудной полости.
На кт очень хорошо видны все сегменты лёгких, благодаря чему, при подтверждении наличия лёгочной болезни, представляется возможным достаточно точно определить область локации заболевания.
Очаги в лёгких на кт
Одним из признаков наличия лёгочного заболевания является образование на лёгких очагов. Стоит понимать, что такая симптоматика присуща в большинстве случаев достаточно серьёзным заболеваниям, которые при отсутствии адекватного лечения могут привести даже к летальному исходу.
Итак, к болезням вызывающим появление очагов в лёгких относят:
- онкологические заболевания, а так же результаты их развития (метастазы, ретикулёз, лимфогранулематоз, непосредственно опухоли и пр.)
- очаговый туберкулёз;
- пневмонию;
- инфаркт;
- эмболию сосудов лёгких;
- отёки в следствии нарушения кровообращения, либо как результат аллергической реакции организма;
- кровотечения;
- сильные ушибы грудной клетки и пр.
В подавляющем большинстве случаев, к появлению очагов на лёгких приводят туберкулёз и пневмония, реже онко- заболевания.
Классификация очаговых образований на лёгких
Сразу после получения снимков кт лёгких имеющих очаги, производится их классификация. На данный момент, в современной медицине очаги классифицируют по следующим признакам:
- Размеры
:
— мелкие (1-2 мм. в диаметре);
— средние (3-5 мм. в диаметре);
— крупные (до 1 см.) - Плотность
:
— плотные;
— средней плотности;
— не плотные. - В зависимости от численности
:
— единичные очаги в лёгких могут быть, как свидетельством такого смертельного заболевания, как злокачественная опухоль, так и обычным возрастным изменением, которое является абсолютно безобидным;
— множественные очаги наиболее присущи для пневмоний и туберкулёза, однако некоторые не многочисленные и достаточно редко встречающиеся разновидности онко. заболеваний так же характеризуются развитием множества очагов; - Месторасположением
. Лёгкие человека покрыты тонкой плёнкой, имеющей название плевра. В зависимости от расположения очага по отношению к ней бывают:
— субплевральные очаги (под плеврой);
— плевральные очаги.
Субплевральные очаги в легких на кт
В современной медицине существует несколько способов диагностики заболеваний лёгких человека: флюорография, рентгенография, а так же компьютерная томограмма.
Для выявления субплевпальных очагов, первые два способа могут оказаться не достаточно действенными, и только использование кт с точностью даст возможность врачу оценить положение больного.
Как отмечалось выше, субплевральные очаги располагаются под плеврой лёгкого. Такая их локация является наиболее типична для таких заболеваний, как туберкулёз и злокачественные раковые опухоли.
Судя по питанию, об иммунитете и своем организме вы абсолютно не заботитесь. Вы очень подвержены заболеваниям легких и других органов! Пора полюбить себя и начинать исправляться. Необходимо срочно корректировать свое питание, свести к минимуму жирное, мучное, сладкое и алкоголь. Кушать больше овощей и фруктов, кисломолочной продукции. Подпитывать организм принятием витаминов, пить больше воды (именно очищенной, минеральной). Закаливайте организм и уменьшайте количество стресса в жизни.
Вы подвержены заболеваниям легких на среднем уровне.
Пока что в хорошем, но если вы не начнете о ней заботиться более тщательно, то заболевания легких и других органов не заставят себя ждать(если еще не было предпосылок). А частые простудные заболевания, проблемы с кишечником и прочие «прелести» жизни и сопутствуют слабому иммунитету. Вам стоит задуматься о своем питании, свести к минимуму жирное, мучное, сладкое и алкоголь. Кушать больше овощей и фруктов, кисломолочной продукции. Подпитывать организм принятием витаминов, не забывайте, что нужно пить много воды (именно очищенной, минеральной). Закаливайте организм, уменьшайте количество стресса в жизни, думайте более позитивно и Ваша иммунная система будет крепкой еще многие годы.
Поздравляем! Так держать!
Вы заботитесь о своем питании, здоровье и иммунной системе. Продолжайте в том же духе и проблемы с легкими и здоровьем в целом еще долгие годы не будут вас тревожить. Не забывайте, что это в основном происходит благодаря тому, что вы правильно питаетесь и ведете здоровый образ жизни. Кушайте правильную и полезную пищу(фрукты, овощи, кисломолочная продукция), не забывайте употреблять большое количество очищенной воды, закаливайте свой организм, мыслите позитивно. Просто любите себя и свой организм, заботьтесь о нем и он обязательно будет отвечать вам взаимностью.

 Вход
Вход